Internacional
Pedirá farmacéutica Moderna la aprobación de su vacuna contra la COVID-19 en Estados Unidos y Europa
Publicado
hace 4 añosPor
SICOM Noticias
El análisis de datos indica una eficacia de la vacuna del 94,1%. Los datos de seguridad continúan acumulándose y el estudio continúa siendo monitoreado por unNIH-Nombrado Junta de Monitoreo de Seguridad de Datos (DSMB).
Redacción
La compañía farmacéutica Moderna informó que planean solicitar este lunes 30 de noviembre una autorización para el uso de la vacuna a la Administración de Alimentos y Medicamentos de Estados Unidos (FDA) y una autorización parcial a la Agencia Europea del Medicamento (EMA).
Anunció que el estudio de eficacia principal del estudio de fase 3 de ARNm-1273 realizado en 196 casos confirma la alta eficacia observada en el primer análisis intermedio.
Asimismo, informó que se detectó una eficacia de la vacuna del 94,1%. Los datos de seguridad continúan acumulándose y el estudio continúa siendo monitoreado por unNIH-Nombrado Junta de Monitoreo de Seguridad de Datos (DSMB).
La empresa dijo que la vacuna tiene un 100% de eficacia en los casos severos.
En total, únicamente 11 personas de todos los participantes en el ensayo quienes recibieron la vacuna se infectaron, frente a 185 en el grupo de placebo, de los que 30 enfermaron gravemente y 1 falleció.
“El ARNm-1273 sigue siendo generalmente bien tolerado; no se han identificado problemas de seguridad graves hasta la fecha“, anunció la empresa.
Te puede interesar
-


Deja actual Gobierno Estatal un Puebla con estabilidad, desarrollo y unido: Sergio Salomón
-
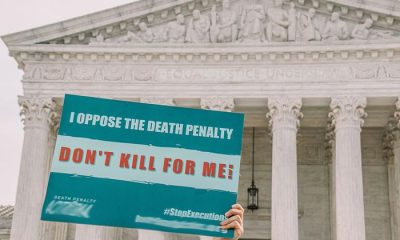

Expertos piden a Estados Unidos que prohíba las ejecuciones con gas nitrógeno en Alabama
-


Lluvias ligeras y vientos fuertes, el pronóstico meteorológico para Puebla este jueves 21 de noviembre
-


Estados Unidos veta por cuarta vez una resolución para un alto el fuego en Gaza
-


Se pronostican lluvias puntuales intensas en Chiapas, Hidalgo, Puebla, San Luis Potosí y Veracruz: Conagua
-


Construyen dos nuevas plantas potabilizadoras en Puebla para mejorar calidad del agua

¡Gloria Trevi cautiva a los poblanos este viernes 22 de noviembre!

Invitan al Primer Foro: “Historia y antropología de la violencia en Chihuahua”


